先駆け腎臓病薬、アルポート症候群でも開発 米リアタが主導、ダブル指定はあるか
糖尿病性腎臓病(DKD)で先駆け審査指定制度の対象に選ばれた協和発酵キリンのバルドキソロンメチル(一般名)について、ライセンス元である米リアタ社が遺伝性糸球体腎炎であるアルポート症候群を対象にした開発を日本でも進めていることが分かった。承認にこぎ着ければアルポート症候群の適応を持つ初の薬剤となる可能性がある。
RareS.コメント
糖尿病性腎臓病に対しての治療薬として第三相試験が開始しており、順調に進めば2022年には申請にたどり着けると予想されているバルドキソロンという薬が、指定難病の「アルポート症候群」に対しても有効性があるのではないかということで、アルポート症候群を対象とした国際共同第2/3相試験が日本も含める形で進んでいます。
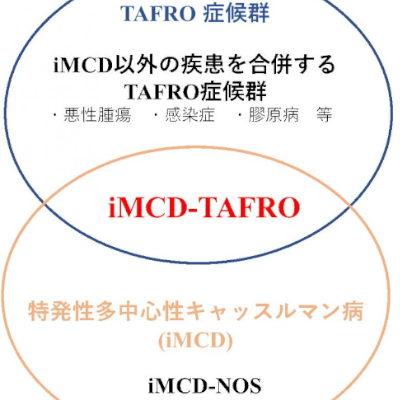
アルポート症候群は、腎臓にある糸球体という尿を作る部分における大事なタンパク質の遺伝子(COL4A3、COL4A4、COL4A5遺伝子)の変異により生じる疾患で、25歳には末期腎不全になるほか、難聴、眼病変などが起きる疾患です。現在は振興を遅らせるための治療、いわゆる保存療法しか存在せず、今回の治療薬が承認されると、アルポート症候群に対して適用を持つはじめての薬となる見込みです。
この薬は、eGFRという腎臓の機能を改善させる能力のあるはじめての薬とも注目されており、末期腎不全だけでなく、膜性腎症やIgA腎症などの他の難病に対しても適用が広がる可能性があるため、期待されています。
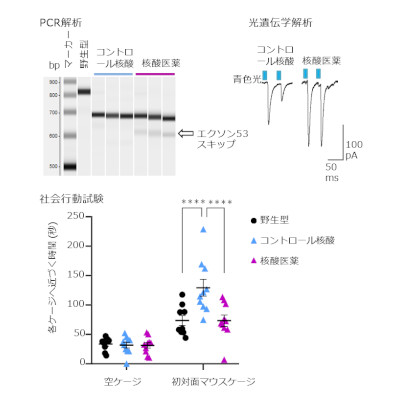
また、アルポート症候群に関しては、日本で行われている別の研究事業で、エクソンスキップを利用した核酸医薬の研究も進んでおり、まだ時間はかかるものの、患者に届けるために薬の開発は今も進んでいます